2024年12月2日�,根據(jù)國家藥品監(jiān)督管理局中國藥品監(jiān)管科學研究行動計劃第二批重點項目“基于遠程/無線傳輸技術的醫(yī)療器械產(chǎn)品的安全有效性評價研究”的要求,國家藥監(jiān)局發(fā)布關于公開征求《醫(yī)療器械遠程傳輸功能注冊審評要點(征求意見稿)》意見的通知�����,一起來看具體內(nèi)容��。
2024年12月2日�,根據(jù)國家藥品監(jiān)督管理局中國藥品監(jiān)管科學研究行動計劃第二批重點項目“基于遠程/無線傳輸技術的醫(yī)療器械產(chǎn)品的安全有效性評價研究”的要求,國家藥監(jiān)局發(fā)布關于公開征求《醫(yī)療器械遠程傳輸功能注冊審評要點(征求意見稿)》意見的通知�����,一起來看具體內(nèi)容�����。
醫(yī)療器械遠程傳輸功能注冊審評要點(征求意見稿)
一�����、適用范圍
本審評要點旨在指導注冊申請人對醫(yī)療器械遠程傳輸功能注冊申報資料的準備及撰寫�,同時也為技術審評部門審評注冊申報資料提供參考。醫(yī)療器械遠程傳輸功能通常是指醫(yī)療器械基于無線/有線通信技術接入網(wǎng)絡��,對醫(yī)療相關數(shù)據(jù)進行實時/非實時聯(lián)網(wǎng)傳輸�����,實現(xiàn)非視距/非接觸的端到端醫(yī)療服務的功能�。本審評要點對含有上述功能的醫(yī)療器械簡稱為“遠程醫(yī)療器械”。
遠程醫(yī)療器械與常規(guī)本地醫(yī)療器械相比主要差異是新增遠程傳輸功能�����,本要點只重點關注新增遠程傳輸功能部分應額外考慮的要求�����。不同遠程醫(yī)療器械應根據(jù)自身技術特點��、預期臨床應用場景滿足相應醫(yī)療器械注冊審查指導原則��、審評要點�、標準等相關文件的要求。
本審評要點是在現(xiàn)行法規(guī)和標準體系以及當前認知水平下制定�����,隨著法規(guī)和標準的不斷完善,以及科學技術的不斷發(fā)展��,相關內(nèi)容也將適時進行調(diào)整�。
二、遠程醫(yī)療器械組網(wǎng)方式
遠程醫(yī)療器械接入網(wǎng)絡有多種組網(wǎng)方式��,醫(yī)療器械注冊申請人可根據(jù)各類組網(wǎng)方式和傳輸方式的特點��,結(jié)合各類遠程醫(yī)療器械的應用目的和場景�,選擇其中一種或多種實現(xiàn)端到端遠程傳輸。
遠程醫(yī)療器械組網(wǎng)方式主要分成以下幾種類型:
(一)廣域網(wǎng)連接場景
1. 蜂窩通信網(wǎng)絡傳輸方式
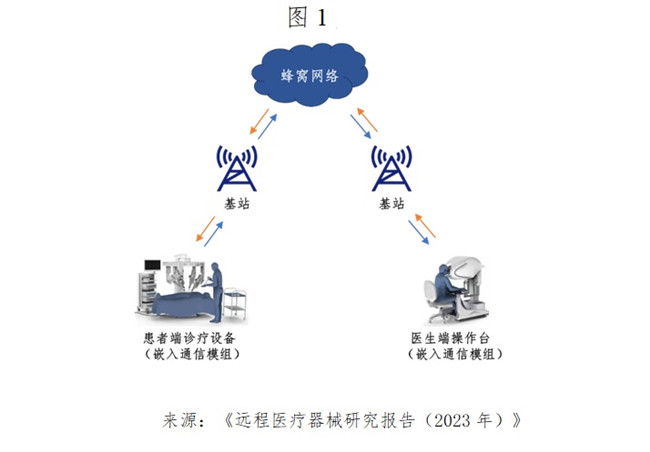
1.1醫(yī)療器械通過內(nèi)嵌4G/5G移動通信模塊連接到4G/5G蜂窩通信網(wǎng)絡��,實現(xiàn)遠程數(shù)據(jù)傳輸和雙向業(yè)務連接��。其網(wǎng)絡拓撲示例如圖1所示��。
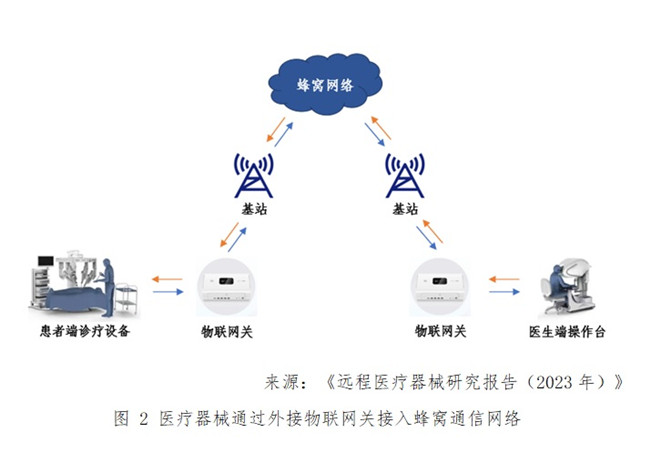
1.2醫(yī)療器械通過以太網(wǎng)線纜/USB線纜/WiFi/藍牙/星閃技術等方式連接到內(nèi)嵌4G/5G模塊的物聯(lián)網(wǎng)關(蜂窩通信網(wǎng)的接入設備)��,再通過物聯(lián)網(wǎng)關接入到4G/5G蜂窩通信網(wǎng)絡�,實現(xiàn)聯(lián)網(wǎng)數(shù)據(jù)傳輸和雙向業(yè)務連接�。這類組網(wǎng)方式的網(wǎng)絡拓撲圖示例如圖2所示。
2. 互聯(lián)網(wǎng)傳輸方式
醫(yī)療器械通過以太網(wǎng)線纜/USB線纜/WiFi/藍牙/星閃技術等方式連接到物聯(lián)網(wǎng)關�,再通過物聯(lián)網(wǎng)關經(jīng)線纜連接到互聯(lián)網(wǎng)接入設備,進而連接至互聯(lián)網(wǎng),實現(xiàn)聯(lián)網(wǎng)數(shù)據(jù)傳輸和雙向業(yè)務連接�。
3. 數(shù)據(jù)專線傳輸方式
醫(yī)療器械通過以太網(wǎng)線纜/USB線纜/WiFi/藍牙/星閃技術等方式連接到物聯(lián)網(wǎng)關,再通過物聯(lián)網(wǎng)關經(jīng)線纜連接到寬帶數(shù)據(jù)專線接入設備�����,進一步連接至運營商的數(shù)據(jù)通信網(wǎng)�,實現(xiàn)聯(lián)網(wǎng)數(shù)據(jù)傳輸和雙向業(yè)務連接。
其中��,物聯(lián)網(wǎng)關的作用主要包括以下一種或多種:實現(xiàn)醫(yī)療器械終端與聯(lián)網(wǎng)網(wǎng)絡之間的接入管理�����、協(xié)議轉(zhuǎn)換和接口適配�����,完成醫(yī)療數(shù)據(jù)傳輸?shù)陌踩用?����,實現(xiàn)多個醫(yī)療器械的并發(fā)接入等��。針對不同的醫(yī)療應用場景�����,物聯(lián)網(wǎng)關需要滿足相關醫(yī)療場景要求,如無菌環(huán)境要求��、強磁環(huán)境要求�����、車載環(huán)境要求等�。
(二)局域網(wǎng)連接場景
在不少非視距/非接觸醫(yī)療業(yè)務中,遠程醫(yī)療器械通過醫(yī)療衛(wèi)生機構(gòu)內(nèi)部或者家庭等應用場景的局域網(wǎng)進行數(shù)據(jù)傳輸�����,局域網(wǎng)可以是覆蓋單個院區(qū)的局域網(wǎng)�、覆蓋多個院區(qū)的局域網(wǎng)、覆蓋家庭的局域網(wǎng)等�。此場景典型的應用包括但不限于:ICU、心臟病監(jiān)護室�、術后觀察室、隔離病房等科室的床旁監(jiān)護設備通過局域網(wǎng)與護士站的集中監(jiān)控設備進行連接�,構(gòu)成非視距/非接觸協(xié)同運行的病區(qū)監(jiān)護系統(tǒng);家庭用的醫(yī)療器械通過局域網(wǎng)與產(chǎn)品的服務站等進行連接�����,構(gòu)成非視距/非接觸協(xié)同運行的系統(tǒng)��。
在此場景中�,遠程醫(yī)療器械通過有線/無線方式連至部署于醫(yī)院內(nèi)部或家庭等場景的數(shù)據(jù)通信設備(路由器、交換機)�,連接方式主要包括:1. 有線線纜直接接入;2. 有線線纜連接至物聯(lián)網(wǎng)關�,通過網(wǎng)關間接接入;3. 短距離無線技術(如WiFi�����、藍牙�、星閃技術、RFID等)接入��。
三��、常見遠程傳輸技術對比
遠程醫(yī)療器械網(wǎng)絡組網(wǎng)方式靈活多樣�����,數(shù)據(jù)在網(wǎng)絡傳輸過程中�,所使用的傳輸技術也是種類繁多,在具體應用場景中��,應根據(jù)每種技術的特點和優(yōu)缺點,結(jié)合應用場景需求�,選擇相應的技術。
幾種常用傳輸技術對比分析如下:
(一)有線網(wǎng)絡具有大帶寬��、低時延和高可靠等特性��。其中:數(shù)據(jù)專線數(shù)據(jù)傳輸性能更優(yōu)(穩(wěn)定可靠)�����,數(shù)據(jù)傳輸?shù)陌踩愿?�,但部署和使用成本高��;互?lián)網(wǎng)數(shù)據(jù)傳輸性能適中�,使用成本最低,但安全性較低�。有線網(wǎng)絡缺點在于不具備移動性和定位能力,無法有效實現(xiàn)醫(yī)院內(nèi)部如病人實時定位�����、監(jiān)護�、移動查房、移動設備管理等移動性強�����、需要準確位置信息的醫(yī)療業(yè)務場景。
(二)藍牙技術是基于低成本的近距離無線技術�����,優(yōu)點在于低功耗�,方便電池供電的設備工作��,價格便宜�����,可應用于低成本的設備�����;缺點在于傳輸距離有限��,傳輸速率低�����,無法滿足高清醫(yī)療影像傳輸?shù)却髷?shù)據(jù)量醫(yī)療應用�����,無法適用于遠程醫(yī)療場景。
(三)WiFi具有布線容易�����、組網(wǎng)靈活�����、可移動和大帶寬等特點�;缺點在于不具備無縫廣域組網(wǎng)能力,無法承載院內(nèi)各樓宇科室間海量設備的接入�����,室外廣域覆蓋不足�����,無法滿足室外醫(yī)療器械終端的接入訴求�����,且安全性低�。
(四)移動蜂窩網(wǎng)絡具有組網(wǎng)靈活�����、可移動�����、運營商統(tǒng)一規(guī)劃部署、抗干擾能力強以及端到端網(wǎng)絡QoS保障等特點�����,支持廣域移動性和便攜性是其顯著優(yōu)點�����;缺點是不易在較大范圍內(nèi)長時間保證其網(wǎng)絡性能的穩(wěn)定性和可靠性�����。
其中:4G覆蓋更廣����,但在低時延和大帶寬上能力不足,網(wǎng)絡室內(nèi)定位能力較差�����,無法實現(xiàn)病人實時定位,無法滿足遠程超高清會診�、應急救援、遠程手術示教等對無線網(wǎng)絡要求較高應用場景的使用需求�。5G具備更靈活、可配置的新型網(wǎng)絡架構(gòu)�、具有十倍于4G的高帶寬、毫秒級的傳輸時延�����,具有更高的連接能力和可靠性����,更適合于對實時性、移動性要求高的遠程應用場景使用����;缺點是目前5G醫(yī)療行業(yè)專網(wǎng)的建設成本和運營成本較高,覆蓋不足�����。
常用無線技術(藍牙、WiFi�����、4G�、5G)傳輸速率、傳輸距離����、時延等性能對比如表1所示。
表 1 不同無線技術性能對比
無線技術 | 傳輸速率 | 傳輸距離 | 時延 |
藍牙 | 1Mbps-500Mbps | 10-240m | 40ms-200ms |
WiFi | 1Mbps-9.6Gbps | 20-300m | 20ms-100ms |
4G | 10Mbps-100Mbps | / | 20ms-100ms |
5G | 100Mbps-20Gbps | / | 1ms-10ms |
四����、遠程醫(yī)療器械通信監(jiān)管要求
遠程醫(yī)療器械是依托通信技術來實現(xiàn)醫(yī)療器械的聯(lián)網(wǎng)應用����,對于含有通信模塊的遠程醫(yī)療器械其本質(zhì)含有電信終端和醫(yī)療器械雙重屬性。對于含有通信模塊的遠程醫(yī)療器械在提交醫(yī)療器械注冊申報前�����,應先根據(jù)《中華人民共和國無線電管理條例》《中華人民共和國電信條例》等文件要求����,取得相關行業(yè)主管部門的許可。
一般而言,具備無線電發(fā)射能力的醫(yī)療器械終端設備(例如:支持蜂窩通信����、WiFi、藍牙等無線技術的醫(yī)療器械終端設備)�����,除部分微功率短距離無線電發(fā)射設備(參見“中華人民共和國工業(yè)和信息化部公告(2019年第52號)”)外����,應當取得型號核準證;具備直接接入蜂窩通信網(wǎng)絡能力的醫(yī)療器械終端設備�,應當取得進網(wǎng)許可證。具體情況建議參考工業(yè)和信息化部相關文件具體執(zhí)行�����。
遠程醫(yī)療器械外接的物聯(lián)網(wǎng)關一般不屬于醫(yī)療器械產(chǎn)品的結(jié)構(gòu)組成����,但遠程醫(yī)療器械使用者應選用已經(jīng)取得相關認證許可后的產(chǎn)品。
五����、審評主要關注點
(一)綜述資料
1. 分類編碼和管理類別
遠程醫(yī)療器械與常規(guī)本地醫(yī)療器械主要差異在新增遠程通信功能����,分類編碼應為原醫(yī)療器械的分類編碼����。管理類別應根據(jù)新增遠程通信功能后產(chǎn)品的整體風險確定,應不低于原醫(yī)療器械的管理類別�。
2. 產(chǎn)品描述
遠程醫(yī)療器械應根據(jù)具體的應用目的、使用場景�����、功能需求�����、安全需求等實際情況����,選擇適用的遠程傳輸方式����。
應明確遠程醫(yī)療器械整體配合工作的原理、組網(wǎng)架構(gòu)�、部署方式、結(jié)構(gòu)及組成、主要功能及其組成部件(如關鍵組件和軟件等)的功能�����、產(chǎn)品圖示(含標識�����、接口�����、操控面板����、應用部分等細節(jié)),以及區(qū)別于本地同類產(chǎn)品的特征等內(nèi)容�。
應明確遠程醫(yī)療器械預期應用的臨床場景(包含遠程推薦使用的臨床情況、術式難度�、遠程端和患者端醫(yī)生的資質(zhì)要求等)和擬解決的臨床需求、所有組網(wǎng)方式(含接入方式和接口要求)����、對網(wǎng)絡性能的最低限要求(例如:產(chǎn)品穩(wěn)定正常工作所需的最低帶寬或最低傳輸速率,產(chǎn)品穩(wěn)定正常工作所需通信信號的最低信號強度和最低信號質(zhì)量����,產(chǎn)品允許的最大時延�、抖動����、丟包率、誤碼率等)�、產(chǎn)品對各種網(wǎng)絡性能劣化和網(wǎng)絡性能受限情形的適應能力、允許的最大用戶并發(fā)數(shù)和形式等����。
應明確進行遠程傳輸?shù)臄?shù)據(jù)類型(如影像、語音����、監(jiān)測信息、控制指令等)�����,對數(shù)據(jù)中包含的信息進行詳細描述����。明確所必須的遠程溝通方式和技術手段����,除音視頻外還需要考慮必要的提示和報警功能����。溝通方式需要兼顧實時性和便捷性����,如應用于遠程手術,還應考慮采用與遠程手術通訊相互獨立的通信線路����,以避免同時發(fā)生延遲或中斷。
對于數(shù)據(jù)傳輸實時性需求較高或者由于網(wǎng)絡性能劣化所致風險較高的遠程醫(yī)療器械�,應明確對網(wǎng)絡性能進行實時監(jiān)測與顯示的功能以及可實現(xiàn)的性能指標,應對網(wǎng)絡異常等情形的機制和能力����,對網(wǎng)絡運行態(tài)勢(例如:網(wǎng)絡異常、網(wǎng)絡劣化����、帶寬受限、網(wǎng)絡擁塞等情形)進行自動感知�、實時監(jiān)測、分析識別����、提示報警和應對處置的功能�����,對主備用網(wǎng)絡/鏈路/路由切換情形的應對機制和能力�����。
此外�,還應提交根據(jù)《中華人民共和國無線電管理條例》《中華人民共和國電信條例》等文件要求�����,取得通信相關行業(yè)主管部門的許可證書����。
(二)非臨床資料
1. 產(chǎn)品風險管理資料
遠程醫(yī)療器械的風險管理應額外考慮加入遠程傳輸功能后產(chǎn)品面臨的網(wǎng)絡安全,數(shù)據(jù)安全�����,數(shù)據(jù)傳輸?shù)耐暾?、時效性,無線共存、網(wǎng)絡異常識別等風險����,并明確相應風險控制措施�����,綜合評價產(chǎn)品風險可接受性����。包括但不限于:
1.1 服務質(zhì)量風險
遠程醫(yī)療器械傳輸醫(yī)療數(shù)據(jù)和控制指令,網(wǎng)絡傳輸性能要求的制定應在滿足臨床使用場景的基礎上�����,充分分析傳輸網(wǎng)絡環(huán)境的不確定性帶來的風險�。對于網(wǎng)絡異常,產(chǎn)品能夠識別并進行報警�,充分考慮各種失效情形(如控制時延過大、圖像卡頓����、網(wǎng)絡中斷等),給出可應對的解決或緩解措施(如性能冗余�����、重新連接、切換備用線路����、患者端本地接管等)和驗證方法,相關研究應覆蓋最不利的情形����。
應充分考慮在實驗室、初次部署與后續(xù)維護過程中網(wǎng)絡環(huán)境的差異����,在上市前建議采用模擬線網(wǎng)(如模擬跨地區(qū)、跨運營商以及多種信號噪聲環(huán)境等情形)進行測試�����。對于可移動應用場景�,應考慮網(wǎng)絡環(huán)境變化(如網(wǎng)關或基站切換帶來的信號強度、信號質(zhì)量變化)帶來的風險�����。
1.2 輻射暴露風險
使用無線傳輸技術的遠程醫(yī)療器械屬于具有輻射或潛在輻射危害且需要安裝的產(chǎn)品�����,應在操作說明中明確有關驗收和性能測試、驗收標準及維護程序的信息����。在可能和適當?shù)那闆r下����,應采取措施減少使用者、其他人員或患者等可能受影響的人在輻射中的暴露�����。
無線傳輸發(fā)射及接收設備產(chǎn)生的電磁輻射可能對人體造成傷害����,產(chǎn)生包括生物效應(如自然流產(chǎn)、胎兒畸形�、DNA變異、染色體異常�、神經(jīng)系統(tǒng)異常等)、致熱效應�、微波傷害(如對人眼造成不可恢復性損害)等風險。
1.3 網(wǎng)絡安全風險
遠程醫(yī)療器械網(wǎng)絡安全風險主要包括身份認證�、數(shù)據(jù)安全保護和用戶隱私保護風險。由于遠程訪問路徑長、節(jié)點多�����,特別是無線信號的廣域覆蓋�,遠程醫(yī)療器械的數(shù)據(jù)和控制可能暴露給更多的威脅參與者。網(wǎng)絡訪問存在通過偽基站����、信號壓制和干擾、空口傳輸及木馬植入等方式�,對網(wǎng)絡中的終端、網(wǎng)管�����、基站和核心網(wǎng)進行滲透的風險�,以及進行非法接入、數(shù)據(jù)竊聽�、數(shù)據(jù)篡改等非法操作的風險。
風險控制措施包括適當?shù)纳矸菡J證機制(如數(shù)字證書)以及數(shù)據(jù)加密傳輸?shù)?����。用戶個人信息在傳輸前應進行脫敏處理�,說明書應告知患者數(shù)據(jù)出院的風險�����。
1.4 使用者風險
使用者的知識背景和操作經(jīng)驗是開展遠程診療的必要條件�。對預期使用者進行充足�����、系統(tǒng)的培訓�,使其掌握相應的技術知識�����、熟悉設備特性并具備各項緊急情況下的處置能力�����,是降低遠程醫(yī)療器械臨床風險的重要方法�。應明確遠端和患者端醫(yī)生的資質(zhì)要求,評價該產(chǎn)品受益風險比�。明確遠端醫(yī)生和近端人員是否需要配合訓練,提供相關的流程和要求�,并基于實際情況考慮可行性。
2.產(chǎn)品技術要求及檢驗報告
產(chǎn)品技術要求應在“1. 產(chǎn)品型號/規(guī)格及其劃分說明”中明確所有組網(wǎng)方式(含接入方式和接口要求)����、允許的最大用戶并發(fā)數(shù)和形式等�。
產(chǎn)品性能指標除了包括遠程應用下醫(yī)療器械自身性能指標外�,具有實時性要求的產(chǎn)品還應包含端到端允許的最大延時要求,網(wǎng)絡實時監(jiān)測�����、報警的要求�����,產(chǎn)品應對各種網(wǎng)絡性能劣化和網(wǎng)絡性能受限等情形的功能要求����,以及遠程通訊中語音和視頻等通訊功能的性能要求(如適用)。并按照《醫(yī)療器械軟件注冊審查指導原則(2022年修訂版)》明確軟件的功能����、使用限制、接口����、訪問控制、運行環(huán)境(若適用)����、性能效率(若適用)等要求�����。
應在附錄中載明對所用網(wǎng)絡性能的最低限要求(例如:產(chǎn)品穩(wěn)定正常工作所需的最低帶寬或最低傳輸速率�����,產(chǎn)品穩(wěn)定正常工作所需通信信號的最低信號強度和最低信號質(zhì)量����,產(chǎn)品允許的最大時延�����、抖動�����、丟包率�、誤碼率等)�。
產(chǎn)品檢驗應在滿足上述網(wǎng)絡性能的網(wǎng)絡情況下進行檢驗,并通過調(diào)整網(wǎng)絡參數(shù)驗證產(chǎn)品在網(wǎng)絡監(jiān)測����、報警以及應對各種網(wǎng)絡性能劣化和網(wǎng)絡性能受限等情形的功能�����。
3. 研究資料
3.1化學和物理性能研究
應明確該遠程醫(yī)療器械所選組網(wǎng)方式����、網(wǎng)絡配置參數(shù)的原因�、臨床意義,考慮引入遠程傳輸技術后對醫(yī)療器械本身����、其他醫(yī)療器械產(chǎn)品安全性、有效性產(chǎn)生的影響�。根據(jù)遠程醫(yī)療器械產(chǎn)品安全、功能需求以及風險分析�,明確組網(wǎng)方式、網(wǎng)絡配置參數(shù)確定依據(jù)�,并提供滿足產(chǎn)品性能、安全要求的所有允許的組網(wǎng)方式下的網(wǎng)絡配置研究測試報告�����。該研究測試應通過模擬線網(wǎng)搭建所有預期允許的組網(wǎng)方式�,通過網(wǎng)絡配置參數(shù)的調(diào)整�,確定出可以滿足產(chǎn)品性能�、安全需求的最低網(wǎng)絡配置參數(shù)。注意研究測試方法應注意客觀性和實用性����,可在能夠屏蔽外界電磁干擾、非預期無線信號和隨機事件干擾的環(huán)境中進行�,配合功能完備且參數(shù)可調(diào)的蜂窩通信實驗網(wǎng)、數(shù)據(jù)通信實驗網(wǎng)絡等網(wǎng)絡設施和專業(yè)設備進行全面精細的驗證和量化評測�,以便構(gòu)造各種不利于醫(yī)療器械的網(wǎng)絡情形,并體現(xiàn)各類組網(wǎng)方式應用中的端到端網(wǎng)絡特性�����。
如產(chǎn)品是變更注冊����,僅是在原產(chǎn)品的基礎上增加遠程應用����。應逐條分析加入遠程傳輸技術后產(chǎn)品性能條款是否受影響,如認為不受影響的條款應結(jié)合設計原理和檢驗方法詳細明確依據(jù)�。
3.2電磁輻射安全性研究
遠程通信模塊與人體距離小于20cm的遠程醫(yī)療器械產(chǎn)品,特別是對于植入�、可穿戴類產(chǎn)品����,使用過程中其電磁輻射暴露可能會對健康產(chǎn)生影響����。針對這部分產(chǎn)品提供相關研究資料或說明。對于植入類產(chǎn)品可參考國際標準組織發(fā)布的ISO14708系列標準中關于電磁場對患者產(chǎn)生的熱傷害防護進行的要求�。
3.3軟件研究
應按照《醫(yī)療器械軟件注冊審查指導原則(2022年修訂版)》《醫(yī)療器械網(wǎng)絡安全注冊審查指導原則(2022年修訂版)》《移動醫(yī)療器械注冊技術審查指導原則》提交相關研究資料。
對于數(shù)據(jù)傳輸實時性需求較高或者由于網(wǎng)絡性能劣化所致風險較高的遠程醫(yī)療器械�����,軟件應具有對網(wǎng)絡監(jiān)測����、顯示、異常識別����、提示和報警等功能,以及相應的備用網(wǎng)絡或應急處理備案的切換要求����。
考慮到遠程醫(yī)療器械的預期用途及使用場景的不同,產(chǎn)品對于網(wǎng)絡安全威脅應具備必要的識別、保護能力和適當?shù)奶綔y����、響應、恢復能力�����。網(wǎng)絡安全能力評價應參考《醫(yī)療器械網(wǎng)絡安全注冊審查指導原則(2022年修訂版)》二十二項醫(yī)療器械網(wǎng)絡安全能力的適用項目進行風險分析�,結(jié)合產(chǎn)品特點應重點關注遠程醫(yī)療器械的適用情況,不適用的項目說明理由����。網(wǎng)絡安全風險評估應進行漏洞掃描,根據(jù)掃描后已知剩余漏洞的內(nèi)容�,分析對產(chǎn)品的影響及綜合剩余風險,確保產(chǎn)品綜合剩余風險均可接受����。
注冊申請人應根據(jù)遠程醫(yī)療器械產(chǎn)品特點、臨床使用場景�����、臨床需求開展數(shù)據(jù)傳輸質(zhì)量研究和數(shù)據(jù)安全研究�。
數(shù)據(jù)傳輸質(zhì)量研究需明確為滿足臨床需求須達到的數(shù)據(jù)傳輸質(zhì)量要求,說明保證聯(lián)網(wǎng)通訊質(zhì)量�、安全采取的措施及相應驗證確認資料,確保傳輸數(shù)據(jù)的完整性����、準確性、時效性����。例如:不同類型數(shù)據(jù)的傳輸機制,分幾路單獨傳輸����,不同數(shù)據(jù)傳輸?shù)膬?yōu)先級保障順序,數(shù)據(jù)傳輸校驗技術����,抖動、丟包率����、誤碼率等要求,以及數(shù)據(jù)傳輸質(zhì)量低于最低要求時產(chǎn)品安全保障措施����,網(wǎng)絡監(jiān)測功能、無線共存等要求和驗證。
數(shù)據(jù)安全研究需綜合考慮隱私保護�����、數(shù)據(jù)加密措施����、攻擊威脅、軟件漏洞�、數(shù)據(jù)可追溯性等風險/需求,明確采取的控制措施和驗證確認資料�����。例如:防止非法接入采取的身份認證�����、通訊加密�����、邀請碼確認等�����。認證內(nèi)容至少應包括控制端/被控制端本地操作者身份(即本地訪問控制)、控制端與被控制端的硬件身份�����,以及控制端與被控制端之間的數(shù)據(jù)傳輸許可����;對于遠程診斷或治療類產(chǎn)品�����,還可包括對手術信息(如手術類型�、患者信息、手術時間)或診斷信息(診斷類型����、患者信息、診斷時間)的確認功能�。身份認證過程應確保合法的操作者和硬件接入到被授權(quán)的遠程連接中。應根據(jù)傳輸數(shù)據(jù)的特性�,對重要的網(wǎng)絡連接過程和遠程控制信息建立日志進行記錄。
3.4動物試驗研究
應根據(jù)遠程醫(yī)療器械預期臨床用途決策是否需要針對遠程傳輸功能開展相應的動物試驗研究�����,并提供論證/說明資料。需要開展動物試驗的應在滿足該產(chǎn)品要求的最低網(wǎng)絡配置參數(shù)的網(wǎng)絡環(huán)境下開展研究�。此外,還需通過模擬斷網(wǎng)或延遲超標等極端情況����,來驗證產(chǎn)品提示、報警后相關應急處理措施預案的可行性以及人員的應急處理能力����,同時對遠程本地互相切換的流程和順暢性進行驗證。
3.5可用性研究
可用性研究應按照《醫(yī)療器械可用性工程注冊審查指導原則》要求在滿足該產(chǎn)品要求的網(wǎng)絡配置參數(shù)下開展研究�����。
4. 產(chǎn)品說明書
遠程醫(yī)療器械說明書中應明確所有組網(wǎng)方式(含接入方式和接口要求)�、對網(wǎng)絡性能的最低限要求(例如:產(chǎn)品穩(wěn)定正常工作所需的最低帶寬或最低傳輸速率,產(chǎn)品穩(wěn)定正常工作所需通信信號的最低信號強度和最低信號質(zhì)量�,產(chǎn)品允許的最大時延、抖動�、丟包率、誤碼率等)����、產(chǎn)品對各種網(wǎng)絡性能劣化和網(wǎng)絡性能受限情形的應對功能、允許的最大用戶并發(fā)數(shù)和形式等�。遠程醫(yī)療器械產(chǎn)品結(jié)構(gòu)及組成中如包含內(nèi)嵌通信模塊�,說明書還應給出已取得的工信部等行業(yè)主管部門認證許可信息�。
對于數(shù)據(jù)傳輸實時性需求較高或者由于網(wǎng)絡性能劣化所致風險較高的遠程醫(yī)療器械,其產(chǎn)品說明書中應當明確網(wǎng)絡不符合預期需求時�����,使用者需要采取的應急措施�����,并將風險告知使用者�����。并提示使用者應確保在遠程醫(yī)療器械使用期間�,保證網(wǎng)絡持續(xù)滿足遠程醫(yī)療器械說明書中的需求�。
還應明確開展遠程操作所需要的人員資質(zhì)和醫(yī)療機構(gòu)的相關要求。人員資質(zhì)應基于相關風險分析進行確定�,手術人員應明確到具體的執(zhí)業(yè)資格、手術經(jīng)驗�����、培訓�、遠近端溝通等����,其他人員應明確資格和數(shù)量要求����;醫(yī)療機構(gòu)所涉及的遠程端和本地端需分別落實相關要求和責任,需確保網(wǎng)絡傳輸條件符合生產(chǎn)商所宣稱的最低標準并采取相應的監(jiān)測措施����。同時給出必要的風險提示和警示信息。
(三)臨床資料
遠程醫(yī)療器械的臨床評價研究可參考《醫(yī)療器械臨床評價技術指導原則》《決策是否開展醫(yī)療器械臨床試驗技術指導原則》《醫(yī)療器械注冊申報臨床評價報告技術指導原則》《醫(yī)療器械臨床評價等同性論證技術指導原則》以及相應產(chǎn)品相關的指導原則開展����。
六、通信相關的名詞釋義
帶寬:頻帶的兩個限定頻率之間的差值�。
傳輸:靠信號將信息由一點傳送到另一點或另外多個點。
傳輸速率:指兩點之間每個單位時間內(nèi)傳送的比特�、字符或塊的平均數(shù)。
時延:信號經(jīng)過某一傳輸路徑所受到的時間延遲����。
抖動:數(shù)字信號的特征瞬間與其理想時間位置的短期非累加偏差。
丟包率:數(shù)據(jù)包傳輸過程中丟失的數(shù)據(jù)包數(shù)量占總數(shù)據(jù)包數(shù)量的比例����。
誤碼率:是指錯誤接收的碼元數(shù)在傳輸總碼元數(shù)中所占的比例����,更確切地說�����,誤碼率是碼元在傳輸過程中被傳錯的概率�����,即�,誤碼率=錯誤碼元數(shù)/傳輸總碼元數(shù)�����。
最大用戶并發(fā)數(shù):當系統(tǒng)提供服務時�,在保證服務質(zhì)量的前提下允許同時接入并服務的最大用戶數(shù)。
注:以上術語參考自《通信原理(第7版)》《GB/T 14733.11-2008電信術語 傳輸》《GB/T 5271.9-2001 信息技術 詞匯 第9部分:數(shù)據(jù)通信》《GB/T 29261.4-2012 信息技術 自動識別和數(shù)據(jù)采集技術 詞匯 第4部分:無線電通信》等�。
七�����、參考文件
[1]國家市場監(jiān)督管理總局.醫(yī)療器械注冊與備案管理辦法�����;國家市場監(jiān)督管理總局令第47號[Z].
[2]國家藥品監(jiān)督管理局.醫(yī)療器械注冊申報資料要求和批準證明文件格式;國家藥監(jiān)局公告2021年第121號[Z].
[3]國家藥品監(jiān)督管理局醫(yī)療器械審評中心.醫(yī)療器械軟件注冊審查指導原則(2022年修訂版)�����;國家藥監(jiān)局器審中心通告2022年第9號[Z].
[4]國家藥品監(jiān)督管理局醫(yī)療器械審評中心.醫(yī)療器械網(wǎng)絡安全注冊審查指導原則(2022年修訂版)�;國家藥監(jiān)局器審中心通告2022年第7號[Z].